製薬企業・CRO・臨床検査会社・スタートアップ向けに、
ER/ES(電子記録・電子署名)対応を含むQMS構築用SOP一式を提供します。
本サービスは単なるテンプレートではなく、
ICH-GCP、21 CFR Part11、Data Integrityの考え方に基づき、
「そのまま運用できるレベル」まで設計された実務パッケージです。
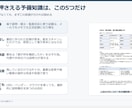
■こんな方におすすめ
・治験を始めたいが、QMSやSOPが整っていない
・ER/ES対応を求められているが、何から手をつければいいかわからない
・監査・査察対応に耐えられる文書体系を整備したい
・ベンダー任せではなく、自社で品質統制を持ちたい
■提供内容(主要構成)
以下のSOPおよび関連資料を一式で提供します。
【上位SOP】
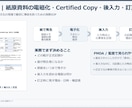
・電子原本/電子署名管理SOP(ER/ES統制の中核)
【下位SOP群】
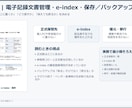
・電子記録文書管理/e-index/保存/バックアップ/移行
・アクセス権限/特権ID/監査証跡レビュー
・変更管理/CSV影響評価/教育訓練/自己点検/ベンダー管理
・紙原資料の電磁化(Certified Copy/後入力/訂正管理)
【補助資料】
・SOP読解ガイド(非専門者でも理解できる解説)
・IMP interface control ガイド
・QMS体制構築手順書(スタートアップ対応)
【新規追加SOPs】
・スポンサー治験オーバーサイト・RBQM/QMP SOP
・委託先資格評価・品質契約・オーバーサイトSOP
・逸脱管理SOP
・TMF/eTMF運用手順書
・CAPA管理SOP
・安全性管理SOP
・データマネジメント統制SOP
・委託先文書受領・返還管理手順書
・アーカイブ保持管理手順書
■本資料の特徴
✔ 実運用ベース(理論ではなく“回る設計”)
✔ ER/ES+CSV+DIを一体で整理
✔ 初心者でも導入可能な構造
✔ 監査・査察を見据えた記録・責任設計
✔ ベンダー管理・権限管理まで網羅
■導入効果
・QMS構築期間を大幅短縮(ゼロ構築 → 即運用レベルへ)
・監査対応力の向上
・属人化の排除と標準化
・ベンダー依存からの脱却
・本資料は雛形ではなく実務設計書ですが、
最終的な適用責任は各社の体制・判断に依存します。
・個別規制・案件への完全適合には追加検討が必要な場合があります。